
Ukrajna és a GMO – Dakotarege
(Géntechnologikaland No78) Ukrajnában a GMO-k társadalmi megítélése összességében óvatos, sokszor elutasító. A közvélemény-kutatások és piaci tapasztalatok szerint a lakosság jelentős...
(Biotechnológikaland No46)
Az új genomszerkesztési eljárásokat a pontosság jellemzi – olvashatjuk szinte minden falvédőn. Ezek a génkonstrukciók felkeresik és azonosítják a célhelyet, és a változtatást ott hajtják végre, ahol terveztük. Első képviselői (hibrid meganukleázok, ZFN-3, TALENs) még jelentős fehérjemunkát igényeltek, így a kivitelezés elég lassú és drága volt. A CRISPR/Cas9 módszernél erre már nincs szükség. A módszer köré speciális tudományos ipar épült ki, amely gRNS-eket és plazmidokat gyárt/gyűjt, továbbá génkönyvtárat épít (Addgene), és minden szempontból kiszolgálja az ezt a technológiát használni szándékozókat. A módszer három vezető egészségügyi cége (CRISPR Therapeutics, Editas Medicine, Intellia Therapeutics) a tőzsdén is megjelent; összértékük egymilliárd US dollár körüli. Mai vezetőik a módszert érintő kritikát olyan módon fogadják, mint a géntechnológia gazdasági sikerében általában érdekelt nemzetközi cégek. Kiemelt céljaik között az egészségügy problémái állnak. Örökletes betegségek gyógyítása, amit emlegetnek, és a személyre szabott gyógymódokról is sokszor esik ismét szó. Az örökletes betegségek kezelését az emberi csíravonal érinthetetlensége miatt moratórium teszi lehetetlenné, bár kínai kutatók erre a területre nem is ritkán betévednek, s a pontosságra vonatkozó PR-szöveget is egyre gyakrabban cáfolják tudományos munkák.

A genomszerkesztési eljárásokkal kapcsolatos hazai lelkesedés most éppen óriási, de úgy látom, hogy a humán-gyógyászatban való alkalmazásukat többen nem látják még elég biztonságosnak. Mi is ennek az oka? Röviden: a célhelyet kerülő (off target) hatások. Járjuk ezt körül. Mindjárt az elején megemlítem, hogy növényekre vonatkozóan olvasható olyan vélekedés, hogy mindez nem olyan fontos, hiszen a szerkesztést követő szelekció a számtalan félresikerült egyedet úgysem tenyészti tovább. Kiválasztja a kevés sikerest, oszt jó napot. Ez kétségtelenül igaz, ha az előidézett mutáció nagyon nyilvánvalóan hibás fenotípust eredményezett. Más a helyzet, ha ez későn és nem külsőségekben mutatkozik meg. Mások viszont azt mondják, hogy a mezőgazdaság kemizálása és géntechnológiai annektálása természetellenes helyzet (monokultúra) normalizálásával próbálkozik. A természetellenes helyzetből fakadó egyensúlytalanság egyensúlyi helyzetét keressük – mi, akik ezt túlszaporodásunkkal és termésmaximalizálási kényszerünkkel kiváltottuk –, vagyis keresünk egy újabb pontot, ami körül szabálytalanul billeg a kvázi-természetes ökológiai rendszerünk.
Emlékszünk Dolly bárány zigótatestvéreinek statisztikájára? 277 próbálkozásból 29 zigóta indult fejlődésnek, 13 implantáció után megtapadt, amiből 5 meg is született. Három hamarosan és egy másik kicsit később elpusztult. Természetesen itt nem genomszerkesztésről volt szó, hanem sejtmag-átültetéses klónozásról. Ami miatt mégsem haszontalan az adatokat idézni, az a tény, hogy a mai géntechnológiai módszerek mindegyike jellemezhető azzal, hogy a módszerünk mennyire pontos és hatékony. Dolly esetében 0,36% volt a felnevelhetőség sikeressége. Nagyon csekélynek gondolom. Hat utódja született később, de élettartama (6,5 éves volt, amikor elaltatták) fele volt a normálisnak. Négyéves korában ízületi gyulladást, majd súlyos tüdőbetegséget (retrovírus okozta tüdőrák) kapott, amely immunrendszerének fejlettségét kérdőjelezte meg. Ezt nem hozták a klónozással kapcsolatba. Az életteljesítménye tehát átlag alattinak minősíthető, viszont ebben a zárt tartás is közrejátszhatott. Minden bizonnyal más kísérletsorozatok (itt emlőmirigysejtekből származott a sejtmag) statisztikája ettől némileg eltérhet. Szívesen olvasnék hasonló statisztikákat a genomszerkesztés egyes módozataival kapcsolatban, hiszen sok dologról árulkodnak ezek az adatok.
Shengdar Q. Tsai hematológus a céltévesztő hatásokat úgy szemléltette egy előadásában (63. ábra), hogy a genomszerkesztés ellenőrzésére van pár rutinmódszerünk, amit átalakításkor használunk. Ezek olyanok, mint a köztéri lámpák. Az ezek fénycsóvájában elveszített dolgokat (értsd indukált mutációkat) meg fogjuk találni, viszont ott, ahol sötét van, ahová a módszereink nem érnek el, esélyünk sincs erre. Ez a véleménye a CRISPR/Cas9 módszerről, amelynek javításán munkatársaival dolgozott és SpCas9-HF1 nevű módszerével ilyen, kedvezőbb eljárást talált is. Véleménye nagyon is a lényegre tapintott – kiterjeszthető a géntechnológia teljes területére –, és mivel a saját esetére talált megoldást, a felbolygatott pro-GM kedélyek gyorsan lecsillapultak.
63.ábra: Az elveszített kulcsok és a közvilágítás esete (S.Q. Tsai ábrája)
Korántsem Tsai az egyetlen, aki a rejtve maradó mutációk miatt azért aggódik, mert a humán-gyógyászati felhasználásnál az onkogén potenciál növekedését feltételezi. 2011-ben Gabriel és mtsai, valamint Pattanayak és mtsi a ZFN-3; 2013-ban Fu és munkatársai, valamint 2017-ben Schaefert és munkatársai a CRISPR/Cas9 módszerek pontatlanságait sorolják. A hibátlannak tűnő elvekből a gyakorlat sokszor tréfát űz; a valószínűtlennek tartott események mégis megtörténnek. Úgy tűnik, a genomi utak mentén a köztéri lámpák még szórványosan pislognak.
Az új genomszerkesztéssel volt kapcsolatos az a 2015-ös vita, amely humán-embriók módosításáról szólt (133. ábra). A kínai szerzők eredetileg a Nature és Science folyóiratokat célozták meg, de azok etikai okok miatt elutasították a szóban forgó cikk közlését. Végül egy kínai újságban jelent meg a közleményük, de a hatás így sem maradt el. Helytálló kérdés, hogy a kiinduló triploid zigóta, amit két spermiummal termékenyítettek meg, diandrikus, vagyis eleve életképtelen vonal, vajon teljesítette-e az emberi csíravonal moratóriumával kapcsolatos kitételt? Azt kell, hogy mondjam, hogy ezek a kísérletek, bár a csíravonal sejtjein folytak, de annak életképtelen mutánsán (a terhességek 2-3%-a eredményez triploid zigótát – ezek csak egy része spermiumtúlsúlyos vagyis diandrikus –, amelyek korai vetélésre/mola-terhességre vezetnek), így az életképes csíravonalat nem érinthették. John Harris megjegyzése nagyon is helytálló abban, hogy az indukált pluripotens emberi őssejtekkel folyó kutatásokat a jelenlegi moratórium nem akadályozza, pedig ezekből másodlagos úton petesejt, vagy spermium is képződhet.
De nézzük a már elkezdett konkrét esetet. A béta thalassemia örökletes vérképzőszervi betegség, amelyben érintettek (Földközi-tenger környéke) nem képesek normális hemoglobinképzésre. Liang és munkatársai CRISPR/Cas9 módszerrel igyekeztek korrigálni a hibás HBB gént. 86 diandrikus triploid embrióba injektálták a mintagént tartalmazó génkonstrukciót. Nyolcsejtes kort 71 embrió élt meg, amelyből 54-et feldolgoztak. 28 volt azon triploid zigóták száma, amelyek megfelelően osztódtak, de ezek közül csak négyben mutatták ki a vegyes mutációt, vagyis a pontmutációt (NEHJ) és a mintaszakasz alapján (HDR) való javítást. Azt találták – ezen túlmenően –, hogy a bevitt konstrukció sokféle és meglepő, nem célzott genetikai problémát is okozott. Ezek aránya sokkal magasabb volt, mint egérmodellen, és diploid emberi testi sejteken korábban találták. Ehhez nyilvánvalóan köze lehetett, hogy a kísérleti célra választott diandrikus triploid humán-embrió osztódási zavarai eléggé gyakoriak. A kísérletet leállították.
Viszont egygénes örökletes betegségek (pl. sarlósejtes anémia, cisztikus fibrózis, Huntington-kór stb.) gyógyításához elkerülhetetlen lesz ezeknek a kísérleteknek az elindítása. Liang és munkatársai szerint az alkalmazott genomszerkesztési módszer nem alkalmas még ilyen változtatások végrehajtására, vagyis humán-gyógyászati feladatok megvalósítására. George Church (az Editas Medicine Inc. egyik alapítója) szerint viszont nem a megfelelő korszerűségű CRISPR/Cas9 módszert használtak a kínai szerzők. Churc doktor mostanában elég sokszor hallatja a hangját; kijelentette, hogy az általa favorizált módszerrel a mamut feltámasztásába kezdtek, amivel kapcsolatban már eddig is sokféle ellenvélemény hangzott el.
133.kép: Humán-embrió (Fotó: Yorgos Nikas/SPS/Nature)
2017-ben Stephen Tsang nyilatkozatai váltottak ki komoly viharokat, amelyek szerint az általuk kifejlesztett módszerrel több ezer nem tervezett mutációt mutattak ki a CRISPR/Cas9 használata után. Az általuk rd1 egérmodellen végzett kísérletben a cél egyetlen nukleotid kicserélése volt. A kezelés gyógyította a génhiba (Pde6b gén) miatti vakságot, azonban 1500 körüli pontmutációt és száz körüli nagyobb változtatás (inzerció/deléció) okozott, amit az erre a célra használt komputerprogram – mint rizikót – egyáltalán nem is jelzett. A szerzők vizsgálataiból levont konzekvenciákat azonnal támadta az Editas Medicine cég, ami azért nem meglepő, mert nagyon sok korábbi eredményt vont kétségbe a cikk állítása, bár a magyarázatokkal adós maradt. Az élénk érdeklődés oka az is, hogy a CRISPR/Cas9 technológia köré kisebb fajta ipar épült mára. A Cowen biotechnológiai részlegének vezetője – aki a ritka betegségek egyik specialistája –, Ritu Baral például igyekezett a közleményt jelentéktelennek minősíteni azzal is, hogy a kísérlet három egérre korlátozódott csupán. Nem ért el sikert: a cikkből pro és kontra vezető tudományos hír lett, amelyhez sokan hozzászóltak.
Az Intellia Therapeutics Inc. és az Editas Medicine Inc. cégek, a CRISPR/Cas9 technológia vezető vállalatai sem hagyták szó nélkül az említett írást. Nessan Bermingham (az Atlas Venture által segített Intellia Therapeutics Inc., a Caribou Biosciences és Novartis partnere) egyszerűen felszólította a cikket megjelentető Nature Methods szerkesztő bizottságát, hogy vonják vissza a cikket. Egyenes beszéd: ami nekik nem tetszik, az ne is létezzen. Én szívesebben vennék kritikát tűrő genomvizsgálatokat, amelyek az észrevett hibákat kiküszöbölve győznek meg. Persze a tőzsdén lévő cégek termékeinek sikeressége nagyban függ a befektetőket ért hatásoktól. A bizalom megingása – amit hasonló vizsgálati eredmények előidézhetnek – a részvények árának csökkenését vonja maga után.
A CRISPR/Cas9 technológia vezető vállalatainak (egyiket sem találjuk a világ vezető biotechnológiai cégei között) tőzsdei értéke egymilliárd US dollár körüli. A vezető biotechnológiai vállalat – Gilead Sciences Inc. – egymaga 138 milliárd US dollár értéket képvisel. A CRISPR Therapeutics AG részvényének árfolyama a napokban (2017. június 21-ei helyzet) éppen a jegyzési (2016. november) árára, ~15 US dollár értékűre zuhant. Az Editas Medicine Inc. részvényára a jegyzési (2016. január) ár alatt van éppen. Az Intellia Therapeutics Inc. részvényei a 2016. júliusi jegyzési árnak messze alatta marad. Eléggé hasonlatos irányok. Átmenetileg csökkentek az árak (most egy hónap után ismét némi emelkedés látok), s ebben a CRISPR/Cas9 technológia esetleges pontatlanságának feltárása játszik szerepet, vagy ennél többről van szó? Nem túlságosan sok már a módszerrel kapcsolatos figyelmeztetés? A CRISPR/Cas9 eljárást végrehajtó plazmidok génpuskával történő belövése teljesíti az irányított mutagenezis követelményét? Szerintem nem. A pontos munkát nem egy nagyon is pontatlan eljárás előzi meg?
A klasszikus és nukleáz bázisú biotechnológiai módszerek gyakorlati összehasonlítása (6. táblázat) számos következtetésre ad alkalmat, amelyek közül a színessel jelzettek emelhetők ki. Ma még – termékeket illetően – a klasszikus növényi géntechnológia uralja a piacot, de a kutatás lassan elfordul ezektől a módszerektől és a nukleáz bázisú genomszerkesztés új változatait használja. Jó irány, de szerintem még csak a kezdeteinél járunk, így nem gondolhatom azt, hogy az EU-nak az Egyesült Államok lelkesedésével azonosulva – hipp-hopp – liberalizálni kellene ezeket a fajtákat. Az új genomszerkesztési módszerek együttes kezelése teljesíti az „esetről estre” való megítélhetőség kritériumát? Nem, semmiképpen sem. Túl sok a megegyezőség még a korábbi módszerekkel. Először talán tapasztalatokat kellene gyűjteni, és bizonyítani a precizitást. Viszont törvényi szabályozásuk átgondolását már most is nagyon helyeselném, amelyhez adok itt pár fogódzót.
6.táblázat: Gyakoribb géntechnológiai módszerek összehasonlítása a növényi géntechnológia példái alapján
Ma már lényegi (mondhatnám kaotikus) a különbség Észak-Amerika és az Európai Unió szabályozással kapcsolatos elképzelések között. Az észak-amerikai engedélyezés egyre inkább a liberalizálás irányába fordul (7. táblázat), míg az EU – szerintem helyesen – nem tágít az elővigyázatosság elvétől. Ez hosszú távon a két kontinens között az élelmiszer-forgalmat lehetetlenné teheti. A nem jelölésköteles, de géntechnológiai úton átalakított növényi termékeket miként ismerhetik fel a kereskedelemben dolgozók? Természetesen sehogy, a fogyasztókat érő meglepetések hamarosan következnek majd. A felsorolásban olvasható kis és nagy deléciók/inzerciók közötti határ vajon hol húzódik? Hiányzik a besorolási elvek közül a felhasznált plazmidok értékelése és sorsának méltatása. Az észak-amerikai engedélyezést ez érzékelhetően nem érdekli, viszont az EU aligha dönthet hasonló módon, vagy egész eddigi szabályozási törekvését az Európai Unió elvetheti.
7.táblázat: Szabályozási eltérések az Európai Unió és Észak-Amerika között (Bruins, 2016 nyomán)
Az Addgene tanácsai a plazmidrendelés előtt több dologra felhívják a figyelmet: (i) a módszer elektroporáción alapul, amivel a plazmidot a sejtbe be kell juttatni; (ii) a bevitelt nagyszámú sejten kell végrehajtani (ez az alacsony hatékonyságra utaló kitétel); (iii) a módszer lentivírust használ. További instrukciók is tartoznak mindehhez.
Stephen Tsang csoportját – vagyis a technológiát használó és publikáló csoportét – érte ezzel kapcsolatos vitriolos kritika is. „Egyértelmű, hogy a szerzők nem szakértők a CRISPR/Cas9 módszerében, a teljes genom szekvenciájában, de a genetika alapvetéseiben sem. Állításuk a ’váratlan mutációkról’ egyértelműen bizonyítják a témára vonatkozó éleslátásuk hiányát.” – jelentette ki az Intellia Therapeutics Inc. csapata. Ez a számomra nem éppen jóindulatú, közösségi (anonim) személyeskedésnek tűnik (személytelensége miatt is súlytalan), merthogy, mint tényállítás, bíróság előtt nehezen lenne bizonyítható, hogy a hat szerző (Kellie A. Schaefer, Wen-Hsuan Wu, Diana F. Colgan, Stephen H. Tsang, Alexander G. Bassuk és Vinit B. Mahajan), akik a Stanford, Iowa és Columbia Egyetemeken dolgoznak, a genetika alapvetéseiben is tájékozatlanok. Miért is kell a szakmai hitelességüket lejáratni? További lehetőségként felmerül, hogy a módszer olyan bonyolultságú, hogy talán csak az előállító cégek szakemberei érthetik a lényegét, használhatják megfelelően és kommunikálhatják az eredményeit. Hihető ez? Ráadásul a CRISPR/Cas9 módszere éppen, mint gyors, olcsó és egyszerűen alkalmazható módszer került be a köztudatba. Mégsem az lenne? Vezető amerikai egyetemek ismert szakemberei sem képesek megfelelően kézben tartani?
Palackposta a törvénykezéshez
Törvénykezés szempontjából a zárt tartású transzgenikus növények/állatok sokkal kisebb környezeti kockázatot jelentenek, mint a környezetbe kibocsájtott egyedek. Növények közül a szigorúan önbeporzók is ide tartozók, de már a vegyes beporzásúak sem. Ez esetben mindig a szigorúbb változatnak megfelelő kezelés szükséges. Megfontolásra édemes azoknak a növényeknek a könnyített kezelése, amelyeknek nemesítése vegetatív alapanyagokra épül, bár rovarmegporzásúak. Növényfajonként, szigorúan kezelve, áru- és vetőmagtermesztésre elkülönítve <0,9% és <0,1% hibridképződési szintre kell az izolációs távolságokat megállapítani. Megengedő törvénykezés esetén a génbankokban való fajtamegőrzést nemzeti felügyeletű, de fajtatulajdonosok által finanszírozott (kötelező befizetésű ügykezelési alapot kell létrehozni a számukra) feladattá kell tenni. A fajtatulajdonosoknak az ügykezelési alapba a kereskedelemben keletkező hasznuk meghatározott részét – illetve, ami arányos az elvégzett munkával – be kell fizetniük.
A hazai előéletet tekintve az idegenbeporzású, magról szaporodó növényeknél a transzgenikus fajták vetését érdemes az EU többi országával együtt továbbra is tiltani. Ez esetben, a GMO-mentes növények (árukat a piac alakítja ki) etetésével keletkező termékek (tej, tojás stb.), mérésekkel ellenőrizhetetlen a GMO-mentességért kért felárakat sokkal szélesebb értelemben kell átgondolni (lásd később) hiszen a vásárló a pénzéért nem kap bizonyíthatóan új minőséget. Igaz a régit (ez az, amit a körötte lévő technológiák ritkává tettek) kapja, amihez fogyasztóként ragaszkodik. A biominősítés ezek közül a legszélesebb kategória, amely természetközeli minőséget kínál, aminek része a GMO-mentesség is. A biominőség feldarabolása szerintem értelmetlen gazdaságpolitikai irány. Ez az, ami az Alaptörvénybe jogilag védhetően foglalható, és a nemzeti fajták kiemelt védelme is. Külön kell kezelni a takarmányozásra és élelmezésre használt GM-állatok és -növények körét, abból a szempontból, hogy van-e a fogyasztásukkal kapcsolatos megalapozott toxikológiai aggály. Ilyen eddig csupán a gyomirtószer-tűrő növények (pl. glyphosate) kapcsán tűnik megalapozottnak, vagyis az Alaptörvény passzusából ki kell venni az ezzel kapcsolatos elővigyázatosságra alapozó, de egészségvédelemre célzó bekezdést, amelyet általánosságban nem erősített meg a tudomány. Ez hatványozottan fontos az egészségvédelmi célú fejlesztések (akrilamid-képződésben gátolt burgonyafajták) esetében. Az Alaptörvény jelenlegi formája szöges ellentétben áll hazánk GM-szója- (nagy része glyphosate-tűrő) importjával, vagyis változatlansága esetén az importot azonnal le kell állítani.
A GM-állatok és -növények kérdését rendeleti úton kell szabályozni, ami sokkal plasztikusabb, a jelen tudásunknak megfelelőbb szabályozásukat teszi lehetővé. A GM-szabályozást illetően a jelenlegi bizottsági alapokra (GEVB) épülő rendszer helyére professzionális háttérintézetet kell létrehozni. Ennek az intézetnek a feladata lehet a géntechnológiára és mellékhatás-vizsgálatokra alapuló (környezetanalitika, ökotoxikológia és dietetika) nyomon követés, a kísérleti kibocsátások és engedélyek kiadása, de amely intézet az ellenőrzés, engedélyezés és jogalkotás-előkészítés funkcióira is képessé kell tenni. Célszerű ezt kutatási alapokra építeni, mert a területi innováció igen intenzív és esetenként nagy bonyolultságú. A szakosított intézet fajtatulajdonosoktól független működtetéséhez stabil állami fedezetet kell biztosítani, amely támaszkodik a fajtatulajdonosok által befizetett ügykezelési alapra.
134.kép: pSC101 plazmid elektronmikroszkópos képe (Fotó: Cohen et al.)
A genomszerkesztési technológiákat tekintve célszerű a génmódosítás (GEO) és az allélmódosítás (GMO) eseteinek szabályozását különválasztani. Nem könnyítésre vagy nehezítésre gondolok, hanem célirányosságra. Az egész genomra kiterjedő vizsgálat végzése fontos feladat, ha a módosítás a csíravonalat érinti. Ez igazolhatja, hogy az előállítás során használt módszer, gének/génrészek nem okoznak eltéréseket a létrejött fajtacsoportban. Megfontolandó a GSO-fajták különválasztása is, amelyek engedélyezésében a létrehozáshoz használt plazmidok (134. kép) bevitelére, működtetésére és sorsára kell koncentrálni. A törvénykezés teljes folyamatát felül kell vizsgálni a GM-állatok területén szerzett jelenlegi tudásunk alapján. A munka sürgős, hiszen a szabályozáson való gondolkodást nem akkor kell kezdeni, mikor az első nem jelölt és nem kimutatható, de géntechnológiai módszerekkel készült nemzetközi fajták és élelmiszerek a kereskedelem révén elérik az EU határait.
A következő rész címe: Genomszerkesztés 8 – Az ipar jogászai megmondják a tutit? (Biotechnológikaland No47)
Darvas Béla
Bankszámlaszám: 12011265-01425189-00100001
Bank neve: Raiffeisen Bank
Számlatulajdonos: Átlátszónet Alapítvány
1084 Budapest, Déri Miksa utca 10.
IBAN (EUR): HU36120112650142518900400002
IBAN (USD): HU36120112650142518900500009
SWIFT: UBRTHUHB
Számlatulajdonos: Átlátszónet Alapítvány
1084 Budapest, Déri Miksa utca 10.
Bank neve és címe: Raiffeisen Bank
(H-1133 Budapest, Váci út 116-118.)
Támogasd a munkánkat az Átlátszónet Alapítványnak küldött PayPal-adománnyal! Köszönjük.
Támogatom PayPal-adománnyalHa az 1 százalékodat az Átlátszó céljaira, projektjeire kívánod felajánlani, a személyi jövedelemadó bevallásodban az Átlátszónet Alapítvány adószámát tüntesd fel: 18516641-1-42
1% TÁMOGATÁS

(Géntechnologikaland No78) Ukrajnában a GMO-k társadalmi megítélése összességében óvatos, sokszor elutasító. A közvélemény-kutatások és piaci tapasztalatok szerint a lakosság jelentős...

(Biotechnologikaland No77) A Marton Genetics Kft. állásfoglalása A Marton Genetics (Bázismag Kft.) cégcsoport a martonvásári kutatóintézet (Agrártudományi Kutatóközpont) munkájára épült....
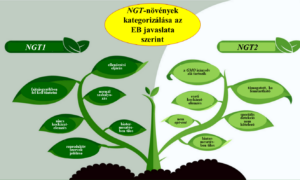
(Biotechnologikaland No76) Előszó A GMO-lobbi hatására az Európai Bizottság javaslata (címábra) komoly visszhangra talált Európában. A javaslatok közül NGT1 esetében...

(Biotechnologikaland No75) Barabás Zoltán Biotechnológiai Egyesület kontra GMO-Kerekasztal A Barabás Zoltán Biotechnológiai Egyesület lépett hazánkban először abból a célból, hogy...
Támogasd a munkánkat banki átutalással. Az adományokat az Átlátszónet Alapítvány számlájára utalhatod. Az utalás közleményébe írd: „Adomány”, köszönjük!