
Ukrajna és a GMO – Dakotarege
(Géntechnologikaland No78) Ukrajnában a GMO-k társadalmi megítélése összességében óvatos, sokszor elutasító. A közvélemény-kutatások és piaci tapasztalatok szerint a lakosság jelentős...
(Biotechnológikaland No45)
Nem emlékszem rá, hogy kívülről (molekuláris genetika) jött technológiára a mezőgazdaság annyi érzelmet pocsékolt volna el, mint éppen a GM-növényekre. A növényvédő szerek úgy hatoltak be ebbe az innovációs vákuumba, hogy ihaj. Ma sem a mezőgazdaság, hanem az európai környezetvédelem és az egészségügy (hazánk hivatalos képviselői nem az élharcosai ennek) ér el változásokat. Az ezredforduló táján, a géntechnológiára alapozva új Zöld Forradalmat is emlegettek néhányan; az éhezés eltörlését és személyre szabott gyógyszereket is ígértek. Euforikus hangulatba kergették egymást a pro-GM aktivisták, aztán Európában egymás után buktak ezek a meseszép – politikusfüleknek szánt – szólamok. Maradtak nekünk a glyphosate-tűrő kultúrnövények és -rezisztens gyomok, a rezisztens kártevők felszaporodása miatt hatásukban amortizálódó Bt-növények és különleges dísznek a lila szegfű. Talán nem is erre gondoltunk. Most, húsz év után új csatakiáltás hangzik. Genomszerkesztés – hallom. Déjà vu. Hatalmas áttörés – állítja a géntechnológiai ipar, és csatlakozik ehhez az USDA és az FDA a deregulációs (könnyített engedélyezési) törekvéseikkel, amitől már Európában is jól meg kell fontolni, miről is van szó. Az EU azonban az eljárások és célok kezelését illetően döntést még nem hozott. A géntechnológia mezőgazdasági eredményei – akárhogyan is szorzom és osztom – elég szerények; mai teljesítményén technikailag még sok a javítandó. Nem pontosak és hatékonyak ezek az új technológiák sem; akad még számos megfontolandó ellenérv; csak az irány pontosabb. Nem jelenti azt, hogy helyes, hiszen az egyensúlytalanságot más egyensúlytalansággal váltja fel. Hosszabb program lesz még ez is, csak szorgalmasan tovább – addig Európában rendületlenül várakozunk –, és teaszünetekben érdemes lehűteni a laborból kikopott, de kommunikációs feladatokban nyomuló agilis kollégákat.

A növényi géntechnológia fejlődése során a lehetőségeinek és az aktuális tudásszintnek megfelelően célokat fogalmazott meg. Mindez folyamatosan tendál a pontosság növekedésének irányába, ami azért várható is. Persze ma az olcsóság is fontos (vö. CRISPR/Cas9) szempont a K+F támogatásában elmaradt országokban, ahol a pályázatokkal a csillagok rutinszerű lehozását is ígérni szokás. Más dimenziók is léteznek. Nem is olyan régen az emberi genomkutatás úttörője, Craig Venter ismét irányt váltott, és a szintetikus biológia bűvöletében élte már az életét, közben az ExxonMobil olajvállalat pénzén (600 millió US$) a GM-kovaalgák révén (Synthetic Genomics) ígérte az olajválság megoldását. Aztán azt mondta túl drága a géntechnológiai megoldás, olcsóbb a bányászott kőolaj, és az öregedés megoldása (Human Longevity Inc.) felé vette az útját. Ez lenne a felhőkarcolók szintje, de mi is történik talajszinten, ahol éppen matatunk. Nem korai még az Alaptörvénybe öntött statikus nemzeti véleményünk? Nem abszurd a géntechnológia minden mezőgazdasági felhasználása felett pálcát törő, megfontolásra sem hajlandó, jogi természetű előítéletünk? Eddig mindig tévesnek minősültek a tudományos törekvésekre végérvényesnek gondolt döntések. Átmeneti korban élünk, átmeneti tudással. Mi történik viszont, ha a tudomány szakít a hagyományos szerénységével, és ipari formáit a gazdaság pillanatnyi érdekeinek szolgálatába állítja. Vesztese ennek a Tudomány hitele lehet, de ez semmi ahhoz a kárhoz képest, amit okozni tud. Nem kellene azt hirdetni, hogy tudásunkban már megelőztük magunkat, mellékhatások nincsenek, csak a lenyűgöző jövő, amit újraszerkesztünk, ahogy éppen tegnap a Plázában láttuk azon a tündéri plakáton.
Ennek a kis sorozatnak a végére hagytam a nekem egyik leginkább érdekeset, ami bejárja majd a transzgenezis és ciszgenezis közötti, nem is csekély távolságot. Itt bujkál szerintem a növényi géntechnológia európai bukdácsolásának a lényege, amely abból az alaptételből indul, hogy minden megoldható („A határ a csillagos ég” – mondták az első ötéves terv ideológusai, s nálunk egy ismert pro-GM vezető is, aki bizonyára nem tudta, hogy kitől idéz), vagyis bármely élőszervezetből (általában a sokat tanulmányozott Escherichia coli és laboratóriumi társai) kiemelhetünk egy gént, és működtethetjük máshol. Sokféle ellenvéleményt fogalmaztak meg ilyesmi kapcsán, amelyek többnyire a korlátozott tudásunkat vették célba. Már sok mindent meg tudunk tenni, csak éppen nem minden vonatkozásában látjuk át azt, amit megtettünk. Szóval a törekvésünk eljuthat oda is, hogy a természetes folyamatoknak megfelelőt hozunk létre, tehát azonos növényből származó alléleket elkülönítve, azokat azonos helyre (locus) bejuttatva. Ez már valóban molekuláris nemesítés lenne, és a génsebészet kifejezés sem hatna nevetségesnek.
Az alább részletezett csoportosítás a tudásunk bővülésével időben sokat változott. Lehet olyan, aki másra emlékezve felfortyan majd. Eltérő szerzők esetleg mást értenek az alatt, amit írok; a jövő bajnokait nem is kalkulálom. Nézzük én milyen fő formákat látok ma elkülöníthetőnek (61. ábra):
61.ábra: A transz-, intra- és ciszgenezis különbségeinek e cikk szerinti értelmezése
Génmódosítások
A célgénre vonatkoztatható természetes genetikai variabilitás (allélkészlet) nem jön létre a befogadó fajban; a célgenomban való specializált locus sem létezik; jól kimutatható módosított élőlények keletkeznek ezen az úton. Esetükben a GEO (genetically engineered organisms) kifejezés lenne helyes, amit géntechnológiai úton létrehozott szervezeteknek fordíthatunk. Formái:
– Xenogenezis – A célsejtbe bevitt génkontrukció elemei a természetben nem léteznek, azt szintetikus úton hozzák létre. A szintetikus biológia ezt az irányt választotta. Átmeneti formák azok (vagyis nem xenogének), ahol a természetben előforduló géneket kurtították meg (a Bt-növényekben többnyire ilyeneket találunk), vagy éppen kiegészítették. A cry-gének kezelésekor elterjedt ez a géntechnológiai gyakorlat.
– Transzgenezis – A célsejtbe bevitt génkontrukció (pl. promóter–operátor–intron–markergén–donorgén–terminátor) a természetben csak összetételét tekintve nem létezik. A transzgén idegen – közeli evolúciós kapcsolat nélküli – sejtekből származik (61. ábra). A szelekciós célú markergén (valahogy követnünk kell az átalakítást) tipikus mellékterméke ennek a technológiának. A kereskedelemben többnyire ezek a fajták kaphatók.
– Linegenezis – A géntechnológia olyan genetikai elemeket használ, amelyben a filogenetikai rokonság a családnál távolabbi, de a kompatibilitás valamilyen formája létezik, s amelyet a klasszikus nemesítők is használnak. Átmeneti kategóriaként – bár itt nincs géncsere, csak epigenetikus hatások – a vegetatív szaporítás (pl. oltás) használhatja ki ezt a lehetőséget. Kihalt fajok interspecifikus klónozásánál is gondolnak rá, ahol viszont már linegén is működhet.
– Famigenezis – A taxonómiai családon belüli génekről (famigén) van szó. Idesorolhatók azok a génkombinációk is, amelyeket laboratóriumi sejt-/szövetkultúrákban (nem ivaros keresztezések) tudunk csak valamilyen genetikai ok miatt (pl. ploiditás) megvalósítani.
62.ábra: Eukarióta 0,2-20 µm hosszúságú homológ kromoszómapár
Allélmódosítások
Itt természetes allélvariabilitás (domináns/recesszív tulajdonságok) létezik, mint a célgenomban való speciális locus/loci (allélhely/allélhelyek) is (62. ábra). Ezek a szervezetek nevezhetők genetikailag módosított szervezeteknek (GMO, genetically modified organisms). Pro-GMO szakértők szerint ez az állapot természetes körülmények, ivaros szaporodáskor is létrejöhet. Önálló szabályozásuk (vagyis GEO és GMO) fontos hatósági feladat lenne. Létrehozásuk módszere a genomszerkesztés valamely formája, amelyben az átalakítást végző plazmidoké a főszerep. Lényeges kitétel, hogy a plazmidok génjeinek/génrészeinek elemei (itt markergének is előfordulhatnak) nem maradhatnak az utódsejt örökítőanyagában. Az allélváltoztatások pozitív és negatív formáit is elkülönítjük, amelyben a negatív változat a csendesítés, amely amint láttuk alapulhat az allél kivágásán, mutációs elrontásán és működésének másodlagos gátlásán is.
– Intragenezis – A faj/alfaj genomján belüli allélkombinációk tartoznak ide. Az allélkontrukció ebből átrendezett sorrendű lehet (61. ábra). Csak a feladat szempontjából nélkülözhetetlen részeket tartalmazza ez az allélkonstrukció, vagyis intront nem feltétlenül. A helyazonos csere itt még nem kitétel. A helyazonosság kitétele transzpozonok (mobilis genetikai elemek) esetében plasztikus szempont, hiszen itt a mobilis elemek természetes mozgásaival bekövetkező helyváltoztatások rendjén valók. Az allélkivágással történő géncsendesítés idetartozik (131. kép). Összetételbeli eltérések és helykülönbözőség miatt is kimutatható.
– Sensu lato ciszgenezis – Az allélkonstrukció az eredeti sorrendnek és összetevőknek megfelelő. A beviteli helye választható, de lehetőleg nem kódoló területekre vonatkozik, vagy olyanra, amit szándékosan akarunk elrontani. Helykülönbözőség miatt genetikai módszerekkel kimutatható változtatás.
– Sensu lato allélcsendesítés – Kivágunk, mutációs úton elrontunk egy allélt (és kópiáit vagy azok közül párat), esetleg RNS-interferencia vagy antiszenz-RNS-technológiával lehetetlenné tesszük az allél működésével kapcsolatos mRNS-tevékenységet. Genetikai módszerekkel nehezen kimutatható változtatás. Gyakorlatilag fontos variánsai tulajdonságaikban esetleg jelentősen eltérnek.
– Sensu stricto ciszgenezis – Locus-azonos allélcseréről van szó, mint az ivaros alapú keresztezésekben is. Genetikai módszerekkel nem mutathatók ki, de gyakorlatilag fontos variánsai eltérő tulajdonságaik alapján felismerhetők, hiszen csak természetazonos részeket tartalmaznak és semmilyen idegen örökítő elemet.
– Sensu stricto allélcsendesítés – Az allél működését gátoljuk, például kapcsolódó mRNS-gátláson keresztül vagy metiláció útján. Nem ismerhető fel, hiszen az utódok reakciója mindenben természetazonos. Számunkra hasznos tulajdonsága alapján felismerhető lehet.
– Markerasszisztált nemesítés – A szülői vonalak allélmódosítása történt meg (lásd fordított nemesítés), de a szóban forgó nemzedékben már nincs nyoma a géntechnológiai beavatkozásnak.
131.kép: Genomszerkesztett csirkék, ahol TALENs módszerrel előzetesen a ddx4-gén került kivágásra, amely ’béranyaként’ hasznosítható állatokat eredményezett
Korántsem állítom azt, hogy az általam felsoroltak merev falakkal elkülöníthető csoportokat képeznek. A különbségek láttatására azonban alkalmas csoportosítás, amit bemutattam. A mai szabályozás már nem tehet úgy, mintha ezek a lényegi különbségek nem léteznének. Kellő mélységben nem tárgyalhattam a géntechnológiai megoldást vezérlő vektorokat (ezek is idegen gének, amelyekről keveset beszélünk), amelyek összetétele és sejten belüli sorsa nagyon is lényeges. Erre példaként említem a CRISPR/Cas9 viaszos kukoricát (DuPont/Pioneer), amelynek létrehozását a fajtatulajdonos részben bemutatta (63. ábra), s amely sokféle gondolatot ébreszthet.
A 63. ábrán lévő plazmidokat génpuskával lőtték be a transzformálásra kijelölt sejtekbe. A plazmidok két gRNS-et hoztak létre, amelyek a CRISPR/Cas9-technológia alapján és a genomban való felismerés után két DNS-törést idézett elő, amely az amilózképződésért felelős Wx1-gént kivágta. 54 gént/génrészt használt ez a fél tucat plazmid, ami a sejtbe egyáltalán nem specifikus úton kerül. A génpuska használata semmiképpen nem biztosíték arra, hogy nem tervezett változások (vö. plazmidtöredékek) ne jönnének létre. Az európai nem GMO státusznak tehát már ezen a ponton sem felel meg ez a fejlesztés. A felhasznált vírus (Enterobacteria fág, SV40) és bakteriális (Escherichia coli, Streptococcus pyogenes) gének többsége nagyon távoli a kukoricától, vagyis transzgének. A létrejött mutánsból hiányzik egy gén (kivágtuk), ami felfogható úgy, mint GMO–-variáns. A fajtatulajdonos a szigorú szelekció során kiválogatta azokat az utódokat, amelyek elérése a célja volt. Valóban nem maradt mit ellenőrizni a hatóságoknak? Valóban lényegi a különbség az eddigi módszerekhez képest? Nekem nem úgy tűnik.
63.ábra: A DuPont/Pioner viaszos kukorica létrehozására felhasznált hat vektor. Félkövér (vastag) betűvel olvasható a konstrukció fontos elemei, amelyek a plazmidokból a Wx1-gén csendítését elérő génkonstrukció részei. Vastag kerettel szedve a kukoricából származó gének/génrészek láthatók. CBI jelöléssel látjuk a cég által bizalmasnak minősített részeket (confidential business information).
Nézzük a problémánk fonákát is. Amennyiben a jelenlegi GMO-szabályozás alá tartoznának a sensu stricto allélcsendesített és ciszgenikus növények, akkor nem lehetne engedélyezni ilyen fajtacsoportokat, mert nem felelnek meg az EU törvényei által megszabott kimutathatóság és jelölhetőség kritériumának. Amennyiben markergénnel kimutathatóvá tennénk ezeket, akkor viszont transzgenikusra rontanánk az eredményünket. Mindenképpen a 22-es csapdája áll elő, vagyis igen fogós kérdés az EU törvénykezése számára. A genomszerkesztéssel előállított növények/állatok is teljesítik azt a kitételt {Cartagena Protocol (Article 3) és EU [(Article 2(2) of Directive 2001/18/EC]}, hogy a GMO az in vitro technika következménye. A géntörvényünk is ezt tükrözi a „géntechnológiával módosított” kifejezés alkalmazásával. A törvényi változtatásokat – ha valamely kormány így döntene – tehát a jogi alapoknál és ott a keletkező termékek elkülönítésénél kell kezdeni.
A hagyományos nemesítésnek bizonyos növényfajoknál is vannak beltartalommal kapcsolatos veszélyei. Azokra gondolok, amelyek toxikus allelokemikáliákat termelnek. A zeller (Apium graveolens) környezeti stressz és betegségek hatására például 8-metoxi-pszoralént (xanthotoxin – furokumarinszármazék) termel, amelyet mutagenitással és speciális esetben rákkeltéssel vádolnak. A nemesített változatokban ez a vegyület alacsony szinten termelődik, vagyis a kockázat felvállalható. Előfordult azonban, hogy a hagyományos nemesítés során létrejött fajtajelölt (a tervezett neve Snowball volt) 8-metoxi-pszoralén-termelése rendkívül magas volt, s a fajtajelölt nem kapott termesztési engedélyt az Egyesült Államokban. Ez azt jelenti, hogy a zeller képes arra, hogy bizonyos allélkombinációban fokozza a metil-pszoralén termelését, és ezáltal emberi fogyasztásra alkalmatlanná váljon. Ez a típusú pleitropikus hatás a ciszgenikus növények esetében is előállhat. Az is tény, hogy a célzott változtatások miatt az erre való számítás esélye talán magasabb, vagyis kiemelt ellenőrzés kérdése a kockázattal bíró növények nemesítése. Hasonló elővigyázatosságot érdemel a burgonya glükoalkaloidja, a szolanin vagy a sárgabarack és a keserű mandula magja az amigdalin (ciántartalmú glikozid) miatt. A gyógynövényekre – ha eléri ezeket a géntechnológiai – mindez hatványozottan érvényes.
A következő rész címe: Genomszerkesztés 7 – Nem létezik olyan, amit nem látunk? (Biotechnológikaland No46)
Darvas Béla
Bankszámlaszám: 12011265-01425189-00100001
Bank neve: Raiffeisen Bank
Számlatulajdonos: Átlátszónet Alapítvány
1084 Budapest, Déri Miksa utca 10.
IBAN (EUR): HU36120112650142518900400002
IBAN (USD): HU36120112650142518900500009
SWIFT: UBRTHUHB
Számlatulajdonos: Átlátszónet Alapítvány
1084 Budapest, Déri Miksa utca 10.
Bank neve és címe: Raiffeisen Bank
(H-1133 Budapest, Váci út 116-118.)
Támogasd a munkánkat az Átlátszónet Alapítványnak küldött PayPal-adománnyal! Köszönjük.
Támogatom PayPal-adománnyalHa az 1 százalékodat az Átlátszó céljaira, projektjeire kívánod felajánlani, a személyi jövedelemadó bevallásodban az Átlátszónet Alapítvány adószámát tüntesd fel: 18516641-1-42
1% TÁMOGATÁS

(Géntechnologikaland No78) Ukrajnában a GMO-k társadalmi megítélése összességében óvatos, sokszor elutasító. A közvélemény-kutatások és piaci tapasztalatok szerint a lakosság jelentős...

(Biotechnologikaland No77) A Marton Genetics Kft. állásfoglalása A Marton Genetics (Bázismag Kft.) cégcsoport a martonvásári kutatóintézet (Agrártudományi Kutatóközpont) munkájára épült....
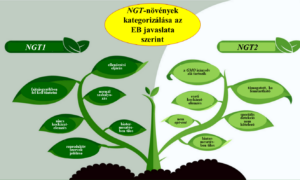
(Biotechnologikaland No76) Előszó A GMO-lobbi hatására az Európai Bizottság javaslata (címábra) komoly visszhangra talált Európában. A javaslatok közül NGT1 esetében...

(Biotechnologikaland No75) Barabás Zoltán Biotechnológiai Egyesület kontra GMO-Kerekasztal A Barabás Zoltán Biotechnológiai Egyesület lépett hazánkban először abból a célból, hogy...
Támogasd a munkánkat banki átutalással. Az adományokat az Átlátszónet Alapítvány számlájára utalhatod. Az utalás közleményébe írd: „Adomány”, köszönjük!