
Ukrajna és a GMO – Dakotarege
(Géntechnologikaland No78) Ukrajnában a GMO-k társadalmi megítélése összességében óvatos, sokszor elutasító. A közvélemény-kutatások és piaci tapasztalatok szerint a lakosság jelentős...
(Biotechnológikaland No18)
A haszonállatokra kiterjedő géntechnológia mindeddig sokkal kevesebb közvitát váltott ki, mint a növényi. Ennek oka, hogy a labor- és haszonállatok zárt tartása, ellenőrzött szaporítása sokkal szigorúbb felügyelet alatt zajlik, mint a nyílt növényi géntechnológia, amely a pollenszórás miatt (idegenbeporzóknál) követhetetlen génelszabadulást eredményez.

A GM-állatok viszonylagos elfogadottságában jelentős szerephez jutottak az orvosi kutatások, ahol egy-egy betegség tanulmányozására már jelentős számú transzgenikus GM-egérvonalat állítottak elő. Az ebbéli kutatások kommunikálása már régen túljutott a média követő képességén, így az ebből származó hétköznapi megítélhetőségen. Nem állítható, hogy nem fogadjuk e törekvéseket is jelentős gyanakvással (igen sok SciFi foglalkozik ezzel a területtel), de a tudományterület sikerének akadályozása szerintem már lehetetlen. Ilyen kísérleteken ugyanis beteg emberek reményei alapulnak, és végül egyéni döntés következik, amellyel szemben általában halálos kimenetelű betegség áll. A kiszolgáltatottság tehát egyértelmű.
Ebben a részben csak a géntechnológiai úton módosított (GM) sertésekre koncentrálok, amelyek a közeljövőben igen sok meglepetést tartogathatnak.
Mielőtt az egyik mondanivalónkra térnénk, járjunk körül egy jelentős problémát. Ez pedig a sertéstelepek trágyakezelése. Egy felnőtt sertés 1,2-2,5 kg trágyát és 2,5-4,5 liter vizeletet ürít naponta. A sertéstrágya sok vizet (75-85%) tartalmaz, amelyben a foszfortartalom (0,4-0,6%), vagyis a legmagasabb a háziállataink között. Egy hízósertés éves trágyatermelését 1,3 tonnára becsülik.
A nagyüzemi tartás során a sertésistállók aljzata rácsos szerkezetű és vízzel mossák (jelentős vízfelhasználással jár) azt a rács alatt lévő csatornába. Így még folyósabbá válik, vagyis a trágya ezt követően ülepítő medencékbe kerül, ahol a hígtrágya-kezelése folyik. A trágyakezelés korántsem mellékes a sertéstartás esetében, hanem megoldandó probléma, amelyben a kilocsolható minőség elérését esetleg speciális készítményekkel is növelik.
Sertések ürülékének foszfortartalma külön gondot okoz, hiszen élővizekbe jutva jelentős alga-felszaporodást eredményez, ami a víz egyidejű oxigénhiányát okozva a halak pusztulásával jár. Gabonafélék korpájában a fitinsav a foszfortárolás leggyakoribb formája. A fitinsav ásványokkal kötött formája a fitát. A fitinsavból a fitáz nevű enzim szabadítja fel a foszfort. A sertés esetében a fitáztermelés hiányzik, így a takarmányban a fitátokkal bevitt foszfor kiürül.
Az Optiphos (Huvepharma) névre keresztelt 6-fitáz, mint géntechnológiai úton módosított (GM) élőlénnyel (Escherichia coli) előállított takarmányadalék európai engedélyezést kapott sertésre és csirkékre. Az EFSA foglalkozott vele a hatósági lapjában (EFSA Journal). Ezt a fitázt egy GM-élesztőgombával, a Komagaetella pastoris állítják elő. Ez az engedélyezett takarmányadalék (Hogy is viszonyul ehhez a hazai GMO-mentesség?) segít abban, hogy a takarmányban lévő fitinsavról lehasítja foszfortartalmú részeket és azokat így felvehetővé teszi. A takarmány foszforhasznosulása (visszatartása) nagyban javul, vagyis az ürülékkel lényegesen kevesebb kerül a környezetbe és okoz majd szennyvíz-kezelési nehézségeket.
A Huvepharma (Bulgáriában alakult magánvállalat, amelynek az Egyesült Államokban is van érdekeltsége) azonban más, nem módosított termékeket is gyárt. Így a Hostazym nevűt, amely nem módosított Trichoderma citrinoviride (gomba) endo-1,4-ß-xilanázt tartalmaz, amely csirke, pulyka és sertés tápokba keverhető. A xilanáz a növényi sejtek hemicellulóz tartalmának hasznosítását teszi lehetővé, amely útján emésztés során hasznosítható xilóz keletkezik. Hasonló készítmény a Xybeten Cell, ami T. citrinoviride endo-1,3(4)-ß glükanáz és endo-1,4-ß xilanáz enzimeket tartalmaz, amely a cellulózemészthetőség hatékonyságát növeli.
A fitáz takarmányadalékkal is bevihető tehát, de a haszonállat-géntechnológia transzgenikus sertésvonalat is előállított, amely nyálmirigyében jelenik meg az Escherichia coli-eredetű fitáz gén (appA), amit egy egérnyálmirigy-eredetű promóter működtet. A szabadalmi bejelentést követően a fejlesztést 2001-ben a kanadai Guelph Egyetem kutatói tették nyilvánossá. A gént tartalmazó plazmidot pronukleusz fázisú embrióinjektálással vitték be (42. kép). A létrehozott GM-sertésvonalban (homozigóta) – amit Enviropig-nek neveznek (43. kép) – a fitáztartalmú nyálelválasztás mérhető. A GM-hímállat a nagy mennyiségű spermiumtermelés és annak raktározhatósága miatt különösképpen értékes ebben a fejlesztésben. Hagyományos vonalakkal keresztezve (hemizigóta) a mendeli öröklődés valósul meg, vagyis a GM-fajta előállítási lehetősége a szabadalmasok kezében tud maradni.
42.kép: Mikronukleusz injektálás – balról a képeken a megtermékenyített petesejtet tartó pipetta, jobbról a tű, amely az 5. pontnál éri el a hím pronukleuszt (Fotó: forrás)
A homozigóta (mindkét szülő módosított appA gént tartalmaz) vonalban tíz nemzedéken át a nyál fitáz-tartalma változatlan szinten termelődött. Az ürülék foszfortartalma 60%-kal csökken. A táphoz külön foszforadalék keverése szükségtelenné válik. Az ilyen sertéstelepek trágyakezelése jelentősen egyszerűbb. A módosított vonalnak – az előállítók szerint – nem változott a növekedési erélye és a húsminősége. Nincs kimutatható különbség a szaporodási paraméterekben sem.
Az eset kapcsán eszembe jut egy lengyel ENSz szakértő, aki Párizsban arról beszélt, hogy sok probléma még csak felvetésre sem került a GM-élőlények szállítása során. Például, hogy minek tekinthető a módosított állat ürüléke, ami gazdag mikrobiális közösség székhelye, amely a szállító vagonokban marad. A nemzetközi szakértői közösség percekig vidáman nevetgélt, pedig akár komolyan is vehette volna a felvetést. A GM-takarmányok emésztésekor a béltartalomban általában kimutatható a transzgén. A transzgén gazdag mikrobiális közösségbe kerül, ahol a spontán DNS-felvétel működhet, vagyis kisebb-nagyobb génszakaszok változatos mikroorganizmusokba kerülhetnek. Ez utóbbiak kifejtésére a lengyel szakértőnek nem maradt már ideje, elsodorta a viccelődő hangzavar.
43.kép: Hemizigóta Enviropig növendékek (Fotó: Univ. Guelph)
A zöld civilszervezetek szerint a sertésürülék magas foszfortartalma csak iparszerű termelés mellett kritikus, így szerintük a tartási forma a megváltoztatandó és nem szükséges ehhez a sertést módosítani. Mindez persze másként néz ki, ha népélelmezési célra szánt húsról gondolkozunk.
2010-ben adták be az FDA-nak az engedélyezési dokumentációt (ez a javított, ún. Cassie vonalra vonatkozott), azonban az további adatokat kért. Legtöbb kérdés ezek közül az Enviropig húsának élelmiszer-biztonságát célozta meg. Ezt természetesnek gondolhatjuk abban a miliőben, ahol a klónozott állatok húsának fogyasztását is előítélet követi, nemhogy a genetikailag módosítottat. A fejlesztést támogató Ontario Pork (évi 1,2-1,3 millió US $ támogatást adott addig) azonban 2012-ben beszüntette a finanszírozást, így a 10. generáció után a tenyészállományt leölték, bár a genetikai állomány (sperma) hosszútávú tárolását megoldották. Az Ontario Pork ugyanis attól tart, hogy az FDA állásfoglalása előtt a vásárlói elfordulnak a húsáruitól – nem tudván, hogy GM-húst még nem forgalmazhat –, mivel nem tudják elkülöníteni a nem módosított termékeiktől. Mindez nem feltétlenül az Enviropig ügyének lezárását jelenti, hiszen az engedélyezési eljárás halad a maga útján és a fejlesztés feltámasztása nem túl bonyolult.
A kullancsok által terjesztett arbovírus (ASFV, Asfarviridae) által okozott afrikai sertéspestisnek ellenálló GM-sertésvonalról valószínűleg hamarosan sokat hallunk majd. Az Egyesült Királyság – Edinburgh Egyetem Roslin Intézete, ahol Dollyt életre hívták – fűz hozzá komoly reményeket. Ez a vírus az immunrendszer speciális túlműködését váltja ki, így annak módosítása vezetett el ehhez a sertésváltozathoz.
Dél-koreai és kínai kutatók viszont olyan sertésvonal kialakításán fáradoznak, amely izmoltsága kétszerese az átlagosnak. A tulajdonság kialakításában a miostatin gén (MSTN) módosított formája játszik szerepet.
Egy éppen induló projekt azt tűzte ki célul, hogy a kasztrálatlan hímek húsa is fogyasztható legyen. A kanszagot (csak ivarérett sertésekre jellemző) valójában két anyag okozza a szkatol (a bélben triptofánból képződik) és az androsztenon, amit sertéseknél a here és a nyálmirigy nagy mennyiségben termel. A nyálmirigy terméke szexferomonként/afrodiziákumként is működik, amennyiben a tüzelő kocák a kan leheletét kimondottan izgatónak tartva ezt viselkedésükkel is kimutatják. Embernél az androsztenont az örökölt receptortól (OR7D4) függően másként érzékelik az RT/RT (vizelet szagot éreznek) és az RT/RW (édes, vaníliás illatot éreznek) génpárossal rendelkezők, vagyis a reakció emberen nagyon is eltérő lehet.
A herélésen kívül megoldásként ismert a vakcinázás (Improvac) is, amennyiben a sertésekbe injekció formájában GnRF-ellenanyagot (gonadotropin releasing faktor) juttatnak be, ami megakadályozza annak az agyi hormonnak a kibocsátását, ami a here androsztenon termeléséhez kellene. Az immunológiai módszerrel való kasztrálás lehetősége viszont felkeltette a géntechnológusok figyelmét is.
Talán a legvárakozásteljesebb géntechnológiai próbálkozás viszont a sertések xenotranszplantációs célra való módosítása. A hibátlan immunrendszer működése miatt azonban még az azonos fajon belül történő transzplantáció (allotranszplantáció) sem egyszerű eset, vagyis a beültetett szerv immunrendszeri válasz alapján való kilökődése előfordulhat. A szöveti inkompatibilitás miatt tehát az alkalmas donorok száma csekély, így a várólista igen hosszú. Így is fontos tényező a hatékony immunszupresszió, aminek gyógyszeres megoldására komoly előrelépések történtek.
44.kép: Páviánba való átültetésre váró, emberszabásúakban xenograft célra módosított GM-sertés tüdeje (Fotó: Chris Maddaloni/Nature)
Olyan könnyen tenyészthető faj használata, amely belső szerveinek nagysága az emberéhez hasonlatos elég korán a sertés felé irányította a figyelmet (44. kép). Kísérleti körülmény között GM-sertés szívét páviánba ültetve az 2,5 évet élt.
A rendkívül összetett xenotranszplantációs munkára céget is alapítottak, amely az eGenesis nevet viseli. A legfontosabb módosítások az olyan fehérjék eltávolítása a sertésből, amelyek az emberszabásúak immunrendszerének válaszreakcióit kiváltják. Első hallásra is igen összetett munkának tűnik. Az ezen dolgozók már húsz körüli módosításon vannak túl, amely a sertésszöveteket elfogadhatóvá teszik az emberi immunrendszer számára, vagyis sajátként ismerhetik fel.
A másik roppant fontos probléma a sertésekben előforduló endogén retrovírusokkal való fertőződés lehetősége. Közülük a gammaretrovírusok (pl. PERV-A, PERV-B, PERV-C) képesek az emberi sejtek megfertőzésére. Ez a terület az FDA érdeklődését is felkeltette. Már a hatvanadik genetikai módosításon túl vannak azok, akik a xenotranszplantációs célra módosított sertésvonalon dolgoznak, hiszen ezek a vírusok a sertés genetikai állományába be vannak ágyazva, így fel kellett ezeket ismerni, majd speciális szerkesztési technikát (CRISPR/Cas9) alkalmazva kivágni a sertésembrióból. A Harvard Egyetem kutatói jelentős áttörést remélnek.
A Revivicor Inc. (Virginia, USA – PPL Therapeutics, UK) reményei jelenleg két területre koncentrálnak. Az egyik a hasnyálmirigy funkcionális szigeteinek átültetése GM-sertésből. Csak az Egyesült Államokban 3 millió cukorbeteg van. Az előkísérletek, ahol makákó volt a recipiens, sikeresnek minősültek. A majmok egy év után gyógyultnak voltak minősíthetők. A másik, szerintük gyorsan megvalósulható reményük a bőr (GalSafe™).
Egy GM-sertésvonal szaruhártyájának emberbe való átültetését 2015. áprilisban, Kínában már engedélyezték. Nem is vitás azonban, hogy a xenotranszplantáció jelentős etikai viták forrása lesz még a jövőben. A sertés szervdonorként való használata az izraelita és muszlim vallásban elképzelhetetlen, de korántsem merítettem ki az ebbéli elfogadás/elvetés lehetséges változatait, hiszen a transzplantáció önmagában sem mindenki számára elfogadható megoldás (nyilatkozó/nem nyilatkozó vallások), beleértve a vérátömlesztést is. Állatvédők az állatok szervdonorként való tenyésztését is ellenzik, bár számomra nem érthető, hogy az élelmiszer céljára való nevelésük/feldolgozásuk miért esne más megítélés alá?
Számomra is súlyos kérdőjel az allotranszplantáció esetében a haldokló válaszának ismeretlensége, ha előzetesen nem nyilatkozott, és a halál elkerülhetetlenségének biztos diagnosztizálása. Papp Lajos szívsebész egyszer azt mondta nekem, hogy az emberi szív cseréje műtéttechnikailag nem túl bonyolult, de etikai okok miatt nem végzett ilyen műtétet, mert dobogó szívet kellene kivágnia, s erre személyiségében nem képes.
A xenotranszplantáció megoldásának választási jogát – amennyiben ez a technológia már felvállalható egészségügyi rizikóval jár – én úgy gondolom a beteg és orvosának döntése kell, hogy legyen. Ezt én az önrendelkezési jogaink közé sorolom.
A következő rész címe: A hatósági döntés társadalmasítása – Géntechnológiai Eljárásokat Véleményező Bizottság (Biotechnológikaland No19)
Darvas Béla
Bankszámlaszám: 12011265-01425189-00100001
Bank neve: Raiffeisen Bank
Számlatulajdonos: Átlátszónet Alapítvány
1084 Budapest, Déri Miksa utca 10.
IBAN (EUR): HU36120112650142518900400002
IBAN (USD): HU36120112650142518900500009
SWIFT: UBRTHUHB
Számlatulajdonos: Átlátszónet Alapítvány
1084 Budapest, Déri Miksa utca 10.
Bank neve és címe: Raiffeisen Bank
(H-1133 Budapest, Váci út 116-118.)
Támogasd a munkánkat az Átlátszónet Alapítványnak küldött PayPal-adománnyal! Köszönjük.
Támogatom PayPal-adománnyalHa az 1 százalékodat az Átlátszó céljaira, projektjeire kívánod felajánlani, a személyi jövedelemadó bevallásodban az Átlátszónet Alapítvány adószámát tüntesd fel: 18516641-1-42
1% TÁMOGATÁS

(Géntechnologikaland No78) Ukrajnában a GMO-k társadalmi megítélése összességében óvatos, sokszor elutasító. A közvélemény-kutatások és piaci tapasztalatok szerint a lakosság jelentős...

(Biotechnologikaland No77) A Marton Genetics Kft. állásfoglalása A Marton Genetics (Bázismag Kft.) cégcsoport a martonvásári kutatóintézet (Agrártudományi Kutatóközpont) munkájára épült....
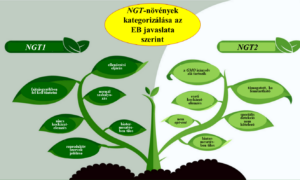
(Biotechnologikaland No76) Előszó A GMO-lobbi hatására az Európai Bizottság javaslata (címábra) komoly visszhangra talált Európában. A javaslatok közül NGT1 esetében...

(Biotechnologikaland No75) Barabás Zoltán Biotechnológiai Egyesület kontra GMO-Kerekasztal A Barabás Zoltán Biotechnológiai Egyesület lépett hazánkban először abból a célból, hogy...
Támogasd a munkánkat banki átutalással. Az adományokat az Átlátszónet Alapítvány számlájára utalhatod. Az utalás közleményébe írd: „Adomány”, köszönjük!