
Ukrajna és a GMO – Dakotarege
(Géntechnologikaland No78) Ukrajnában a GMO-k társadalmi megítélése összességében óvatos, sokszor elutasító. A közvélemény-kutatások és piaci tapasztalatok szerint a lakosság jelentős...
(Biotechnológikaland No43)
Szeretnék sokkal optimistább lenni. Szakmai ártalom nálam, hogy kiszúrom a dolgok gyönge pontjait. Az oligonukleotid-irányított mutaganezis (ODM) nevű technológia Európában nem csak nekem tűnik egyszerű (gén)barkácsolásnak. Az Egyesült Államok döntéshozói szerint persze rendben lévő módszer ez, sőt nem is GMO, ami ezen az úton jön létre. Az EU viszont – úgy tűnik – erre is nemet mondott. Nehéz elhinnem, hogy ezek a mutációt indukáló nukleotiddarabok csak ott avatkoznak be, ahol azt számukra terveztük. Az örökítő rendszer ennél talán bonyolultabb. Specifikus tehát ez a módszer? Mennyire? Mik a pontos mutatói az egyes konkrét eseteinek? Az egész genomra kiterjedő vizsgálatokat esetről esetre meg kellene követelni ilyenkor, ha termékig jut egy fajtatulajdonos. Megalapozatlan kérés ez, ha egy faj csíravonalához nyúlunk? Miért csak az ember csíravonala tabu? Nem számtalan szálon függünk attól az életközösségtől, amiből kiemelkedtünk? Súlyos ellenérzésem van a gene drive nevű génvezérléses fajpusztítás módszerével is. Nem azért, mert bukolikus hangulatban néha elsiratom a vérszívókat. Kimondottan bajom van velük. Viszont innen-onnan összegereblyézett gének örökíthetően öngyilkos sorrendbe helyezése már határozottan nem lelkesít. Az sem, hogy ellenszer is tervezhető. A még egyenlőbbek ekkor szaporodhatnak. Valóban át akarjuk alakítani a földi élővilágot? Valóságot jósló scenario a Prometheus című filmé? Lehet, hogy Godot egyszer – mikor már nem is várjuk – mégis, és ebben formában érkezik meg? Töröl, majd újranépesít, mert megérdemeltük?

Az első generációs, többnyire növényvédelmi célú fajtacsoportok és a helyspecifikusnak tűnő genomszerkesztési eljárások után fussuk át a többi említett genommódosítási módszert is, ami ma elég gyakori előfordulású ahhoz, hogy meg kelljen értenünk.
Oligonukleotid-irányított mutagenezis alapú genomszerkesztés – ODM
Akaratlanul a nyolcvanas évek OMD (Orchestral Manoeuvres in the Dark) nevű zenekara jut eszembe. Egyrészt a betűszó rövidítése, másrészt az áthallás miatt: zenekari műveletek a sötétben. Nyolcvanas évekbeli szinti-pop; akkor meghökkentő, ma inkább mulatságos.
Az ODM (oligonucleotide-directed mutagenesis) technológia viszont rövid – felismerési célú – nukleotidszakaszok használatán alapul, amelyek pontmutációkat hoznak létre a genom komplementer szakaszán. Az eljárásban 20-100 bázisnyi, a célzott növényi genomszakasz bázisszekvenciájától csekély mértékben (egyetlen bázisban – ez a pontmutációt kiváltó rész) eltérő oligonukleotidokat juttatnak a célsejtbe. Elárasztják vele, ahogy valahol olvastam. A bejuttatás módja a klasszikus módszereknek megfelelően indult, azaz szívesen alkalmaztak génpuskát (ekkor persze sérülhet is a lövedék), és a felismerés céljára fluoreszkáló markert, ami a mikroszkóp alatti felismerést teszi lehetővé.
A tervezett oligonukleotidok megtalálják a megváltoztatásra kiszemelt szekvenciát (szekvenciákat?), hozzákapcsolódnak, és DNS-törést okoznak (54. ábra). A sejtek hibajavító enzimei ezt észlelik, és a javító tevékenységük nyomán a bevitt oligonukleotid-szekvenciát tekintik mintának. A nukleotidcsere új mutációt eredményez, de létező (néhány nukleotidnyi) mutáció is elvileg megszüntethető. Mindeközben a tervezetten mutagén oligonukleotid elemeire hullik. Egyesek szerint az idealista álom itt ér véget. Többek szerint a technológia korántsem precíz, éppen ellenkezőleg az indukált DNS-törések miatt kifejezetten mutagén módszer, amelyben a célsejt DNS-javítási mechanizmusa állítja elő az új változatokat. Az ODM módszere a termékfüggetlen civilszervezetek szakértőitől már eddig is erős kritikát kapott.
54.ábra: Oligonukleotid-irányított mutagenezis alapú genomszerkesztés (van der Meer nyomán)
Az első kérdésre más kitértem. Eléggé pontosak vagyunk-e? Nos, a genomban több azonos/hasonló örökítő hely lehet, amit a jelenlegi módszerek még nem tudnak pontosan elkülöníteni. A szorgalmas innovátorok – különösen nálunk – türelmetlenül tekintenek azokra, akik az ő munkájukban nem a haladást, hanem a fennmaradt problémákat veszik észre. Nézzük azért a minimális programot (egygénes mutáció), mint második fő kérdést. Valóban ez akár kívül is eshet a GMO-szabályozás hatáskörén (az Egyesült Államokban ez történik éppen), hiszen elvileg egy allél változását/mutációját értük el. Valóban csak ennyit? Nem következett be a genom más helyén nem tervezett mutáció? Nem kérdéses a módszer szelektivitása? Nem gyanús a módszer pár százalékos hatékonysága (átalakítás frekvenciája), amit a mi kijelölt célunk szerint mérünk? Tipikusan olyan esetnek látszik ez nekem, amelynél a genomanalízisssel való bizonyítás nem elkerülhető. Hogy kémiai mutagenezissel előállított fajtáknál ez miért nem volt kritérium – csak a kanadai engedélyezésben –, azt ne tőlem tessék kérdezni. Az európai döntéshozók akkor talán – a mai tudásunk szerint – tévedtek.
Az egy allélre korlátozódó változtatást mindaddig tarthatjuk elviselhetőnek, amíg azt feltételezzük, hogy ezek az egységek egymástól függetlenül működnek. Természetesen nincs így: a ’szervezet’ szavunk is azt közvetíti, hogy sokféle aktivitás rendezett összjátéka eredményezi az életképes egyedet. Egy fehérjében bekövetkező egyetlen változtatás is ún. pleitropikus hatást indíthat el, vagyis szerteágazót, hiszen funkcionálisan az érintett fehérje eltűnhet/megváltozhat, és ez az állapotváltozás jellemzi a további kapcsolatrendszerét. Ha valamely enzimre vonatkozik ez a változtatás (vö. géncsendesítés), akkor a hatás nagyon is látványos lehet: nem barnul például a feledékenyen félbehagyott alma. De tényleg meg kell ezt a súlyos problémát géntechnológiai úton oldani?
Másfelől viszont az egygénes mutációk szerves részét képezik az evolúciónak. Az élőlények változása/fejlődése ezen alapul. Még ma is tengeri szivacsként tapadnánk a tengeri talapzathoz, ha nincs mutáció – mondhatja bárki. A napfény UV-sugarai – ez már csak természetes – is ilyen hatásúak. Mi abban az extra, ha a változtatásokat az ember hajtja végre? Talán, hogy szabályozással könnyen elkerülhetők. Az ember által módosított evolúció kezdődik mától? Az ember a megszerzett tudásával és laboratóriumi munkájával nem része a baljós Természetnek? Mindenképpen az. Akadhat-e ebben a megközelítésben nem tervezett hiba? A mutációk nagyobbik része káros; egyedek és csoportok pusztultak ki új patogének miatt az elmúlt évezredek alatt (124. kép). Tudjuk, hogy a mai életformák szempontjából a mutációs arány optimálisnak tekinthető. Evolúcióteoretikusok szerint kisebb mérvű mutáció mellett túl lassú lenne az evolúciós folyamat, nagyobb mutációs ráta viszont az élet – legalább is most ismert formái – pusztulásához vezetett volna. Indokolt ekkor az európai elővigyázatosság elve? Azt gondolom, hogy messzemenően igen. Lehetne kritikusan szemlélni a vágyainkat (vö. születésszabályozás), nem kellene talán mindent most és egyszerre akarni (vö. fenntarthatóság). A megfontolt szemlélődés szerintem még sohasem ártott.
124.kép: A hatodik tömeges fajpusztulás előtt? – Kígyók és koponyák (Fotó: Adam Cohn/Flickr/Business Insider)
Az ODM technológiához tartozóan a BASF és a Cibus nevű cég RTDS (Rapid Trait Development System – gyors tulajdonságfejlesztési rendszer) néven jegyzi azt az átalakítási módot, amellyel szulfonilkarbamid-tűrő olajrepcét állítottak elő. A SU Canola nevű terméket nem GMO-ként hirdeti a Cybus honlapja. Joggal, ugyanis 2015-ben az Egyesült Államokban nem GMO kategóriába helyezték, és 2016-ban Kanadában – ahol a mutációval előállított fajtákat is külön követik – is engedélyt kapott. Az ISAAA úgy jelentette be, mint az első genomszerkesztéssel készült, nem GMO fajtacsoportot. Az EU szerint viszont ezzel a technikával előállított növények egyértelműen a GMO kategóriába tartozók, és nem a mutációs nemesítés termékei, amelyekre a fajtatulajdonos furfangos szóvivői hivatkoznak. Elérkeztünk, tehát egy újabb szakító ponthoz az Egyesült Államok és az EU GMO-kal kapcsolatos engedélyezési felfogása között. Mindez a CETA– és TTIP-jellegű keretmegállapodások tekintetében jelentős problémaként mutatkozhat a jövőben.
Vajon mi lehet az oka a teljesen eltérő vélekedésnek, amelyben az EU tagországai egyre inkább az elutasítás indokait keresik? Én azt feltételezem, hogy az Egyesült Államokban a fogyasztók igen sok dologra nem fordítanak figyelmet. A világ sikeres államában élnek, kételkedés/mérlegelés nem a dolguk. Nincs is olyan széleskörű a tudásuk, amire alapozhatnának. Életemben rengeteg szakbarbár, érdeklődési és belátási körében korlátozott (egy ügyű) kutatóval találkoztam. Svédországban a Karolinskán lepett meg az a közhangulat, hogy ez utóbbi mesterfélét miként különböztetik meg, és nem hívják sohasem társaságba a vezetőik. Unalmas, mondanivaló nélküli emberek – mondta nekem az egyébként megfeszített munkájukért hálás főnökük. Rémületesnek tűnt a dolog. Nem elégséges szorgalmasnak lenni, még eredeti egyéniségre is szükség van? Viszont a tudomány valójában az intuícióról szól, arról a képességről, ami nem tanítható, hogy sok apró részletből megsejtsd mások előtt a képet. Ez az eredeti felé való törekvés valóban messze több (stimulálóbb) annál, mint ami az általam nagyon is tisztelt szorgalommal megszerezhető.
Nincs jelölési kötelezettség Észak-Amerikában, vagyis a fogyasztók ebben a tekintetben tájékozatlanok. Bíznak abban, hogy eddig is sikeres vezetőik jó döntéseket hoznak; nem kell fárasztani magukat a nyomozással. Persze ebből az önfeledt gyanútlanságból lehet csak mélyen csalódni. Európában más a helyzet. A történelmi előéletünk messze bonyolultabbá tette azt az érzést, amit feltétel nélküli bizalomnak nevezünk. Egyre ritkábban használt szavunk ez, mint minden olyan szó használata is, ami erre épül. Bizonyítékokra várunk minden területen. Körbe kérdezzük, ami előtt elfogadunk valamit. Gyanús, ami gyorsan közeledik; gyanús, aki ennek tökéletességéről fecseg. Kételkedem, tehát gondolkozom (Dubito ergo cogito). A létezés ehhez képest átmeneti állapot. Nálunk jelölés van, s amit megjelölnek, az felkelti az érdeklődést.
Fajfenntartást támadó genomszerkesztés (gene drive)
Nagyobb népességeket (esetleg fajt) érintő géntechnológiai lehetőség, ami elég általános örökítő folyamatot támad ahhoz, hogy figyelemre méltassuk. Ma a legsúlyosabb bioetikai kérdéseket felvető géntechnológiai változat, amellyel elvileg egy célzott faj teljes kipusztítását is elérhetjük. Ma még a betegségterjesztő (zikavírus) csípőszúnyogok a célpont, de már mezőgazdasági rovarkártevők is kiszemeltek. Ma még érteni véljük a célt, de egyidejűleg mérlegelhetjük is. Az idegenkedők általános etikai alapkérdése az, megengedhető-e olyan géntechnológiai módszert szabadon engedni, amelynek kifejezett célja, hogy adott faj(oka)t kipusztítson. Persze nem eszik a kását olyan forrón, hiszen egy rovarfaj sok elszigetelt népességből áll, amelyek között a géncsere nem valósul meg egykönnyen. A módszer más kritikusai nem néhány rovarfaj kipusztítása miatt aggódnak, nem is a csípőszúnyogokat fogyasztó madarakra mutogatnak, vagyis az ökoszisztémában keletkező zavarra, ami egy lényegi forrás kiesésére sokféle változással kell, hogy reagáljon. A rendszerre jellemző a messze hullámzó hatás.
55.ábra: A gene drive alapesete. Endonukleáz enzimet kódoló génszakaszt viszünk be az egyik szülőbe, amely a heterozigóta egyedekben a módosítatlan nukleotidpárnál vág, majd átmásolja (homológia irányított javítási mechanizmus, HDR) magát. Előfordulhat még, hogy az átmásolás helyett pontmutáció jön létre (kapcsolódás a nem homológ végen, NHEJ), vagy a vágás elmarad (Esvelt et al., 2014 nyomán)
A félelem forrása sokkal inkább az, hogy mi van, ha ez a tervezetten önpusztító rendszer kikerül a rovarokból, és csekély módosításokkal átkerül (vö. bioterrorizmus) más fajokba? Az örökítőrendszer hasonló működése a földi szervezetek esetében ezzel a súlyos veszélyeztetéssel jár. Az alapgondolat, hogy olyan örökítő anyagot viszünk be a sejtbe (55. ábra), ami a csíravonalban öröklődik (ez eddig az emberben tabu), s az többnyire képes átmásolni magát (HDR), majd az örökítőképességet így sokszorozva (az érintettek többsége homozigóta hordozóvá válik – 56. ábra) az utódok fejlődéskori életképtelenségét elérni. Elképesztő gondolat, a fajkipusztítás receptje. Nézzük a ’Prometheus’ bevezető képsorait: a bolygóra szállított Kiválasztott iszik egy szelencéből, majd a DNS-ei felszakadnak, a szervezetének nagyobb darabokra hulló örökítőanyaga a vízbe kerül (címkép), ahol újra indítja az Evolúciót, ami előtt – ha jól gondolom – a korábbi életformák eltörlése áll.
56.ábra: A csíravonalba bevitt gene drive által nemzedékenként érintett egyedek aránya (Esvelt et al., 2014 nyomán)
Az Oxitec nevű brit cég mutatta be (57. ábra) a rovarok ellen való védekezésnek ezt az alternatíváját, amely rokon ugyan a sterilhímes technológiával, de valójában nem kötődik az ivarokhoz, bár itt is hímeket bocsátanak ki. A párzások után az utódokban a génkonstrukció tTAV-génje toxikus fehérjét termel, amely kötődik a tetO7-kötőhelyhez és további tTAV-fehérje termelésére serkent a konstrukciót. A tTAV-fehérje a legkülönbözőbb génekhez kötődve blokkolja azokat, megakadályozza az élethez szükséges fehérjék megjelenését, és még lárvakorban pusztulást okoz. A tTAV-fehérjéhez azonban tetraciklin kötődhet, ami leállítja a folyamatot, vagyis a tetO7-kötőhely üresen marad és a tTAV-gén működése leáll. A lárvák a tenyészetben normálisan fejlődnek. A szúnyogtörzs fajfenntartása tehát tetraciklin-függővé vált, csak azzal van esélye. Kibocsátáskor a letális génkombináció az öröklődés szabályainak megfelelően jelenik meg a népességben, és ott felgyarapodva kipusztítja azt. Ezzel egyidejűleg az utódpusztító génkontrukció önmagát is felszámolja, vagyis az izoláltan élő szomszédos népességet érintetlenül hagyja, ha az aktív terjedőképesség nem túl nagy. Csípőszúnyoknál ez a helyzet, bár a passzív terjedés itt kifejezetten ismert, amikor egy felszálló légáramlat a népesség tekintélyes részét felemeli, majd nagy távolságra szállítva kiszórja.
57.ábra: Az Oxitex módszere GM-Aedes aegypti előállítására
Fordított nemesítés (RB)
A fordított nemesítés (reverse breeding) során a jól teljesítő heterozigóta elit hibridből állítjuk elő – géntechnológiai közvetítéssel és szövettani munkával – a szülői homozigóta vonalakat. Mindez meglehetősen komplex feladat, amely a nemesítői módszereket kombinálja (58. ábra). Nevezhetjük a génmarkerezéssel (marker assisted selection) végzett nemesítés alesetének is. A nemesítés közbenső fázisában tehát géntechnológiai beavatkozásra kerül sor, amikor a kiválasztott egyed sejttenyészetében géntechnológiai úton jelöljük a kromoszómákat. A létrejött haploid sejteket doubled haploid osztódásra bírjuk (pl. colchicine-kezelés). A zigóták közül a jelölt szülői vonalakat eltávolítjuk, míg a két módosítatlan szülői vonalat regeneráljuk. A létrejött stabil (rekonstruált) elit vonal már nem tartalmaz géntechnológiai módosításokat, vagyis nem ismerhető fel ilyennek. Jelenleg kis genomú, diploid növényfajok kezelésére alkalmas ez a módszer. A termék az Egyesült Államokban nem GMO státuszú. A módszerrel előállított fajták nem ismertek (ez bejelentésen múlna), de a helyzet az, hogy mindez az európai engedélyezés miatt lehet így, mivel a transzgenikus növény nem GMO utódja is engedélyezési/nyilvántartási eljárás alá esne. Az RB megfelelő végrehajtása nem ad lehetőséget a felismerésre.
58.ábra: Fordított nemesítés (RB) vázlata
Egyéb géntechnológiai megoldások
Ezekben az esetekben nem külön géntechnológiai módszerekről van szó, hanem speciális alkalmazásokról.
– Oltás GM-alanyra
A GM-alanyra nem GM-növényt oltanak. Ez főként talajból származó betegségek és kártevők ellen látják használható eszköznek. A GM-gyökér (telepítése engedélyhez kötött) és módosítatlan oltvány közötti anyagszállítás megvalósul, de örökítőanyag nem kerül át az oltványba, így az oltványon termő rész Észak-Amerikában nem GMO minősítést kap. Citrusféléken alkalmazott módszer. Európa a nyilvántartás irányát választotta.
– Agroinfiltráció
A teljes nevén Agrobacterium-infiltráció során a növénybe (levélkorong, növényi sejt) transzgénnel módosított Agrobacterium-szuszpenziót juttatnak, így érve el ott a transzgén kifejeződését. A módszert nagyon gyorsnak tartják, de használatát főként a vakcina- és antitesttermelő növények területén kutatók szorgalmazzák. Ehhez a területhez hozzátehetjük, hogy már a növényi géntechnológia hőskorában olvashattunk a módszerről, de termékeinek kritikai adatbázisban való megjelenése várat magára. A gyógyszerészet régóta a saját (No trespassing) útját járja, s nem nagyon tart arra igényt, hogy termékeibe a széleskörű nyilvánosság belelásson. Pedig, ha valaki a rákkeltéssel gyanúsított hatóanyagok listáját (IARC) kézbe veszi, minden bizonnyal meg fog döbbenni azon, hogy mennyi gyógyszer-hatóanyag található közöttük (pl. azathioprine, cyclosporine, chlorambucil, melphalan, tamoxifen, chloramphenicol, phenobarbital, cisplatin, adriamycin, phenolphthalein, griseofulvin, metronidazole, sulfasalazine, nafenopin, dacarbazine, bleomycin stb.), amikre a szülei múltjából még emlékezik.
Növényvédelemben a rovarvektorok (pl. növénytetvek) által terjesztett növénypatogén vírusok a gyümölcsfélékben a géntechnológia érdeklődését is magukra vonzották. Az agroinfiltráció módszere ezeknek a vírusoknak a növényi sejtbe való bejuttatására is képesek úgy, hogy nincs szükség a helyzetet komplikáló rovarvektorra.
– Szintetikus genomika
A szintetikus genomika mindazon genomikai módszereket foglalja össze, amelyek természetben nem létező összetevők és rendszerek létrehozására irányulnak. Ez esetben már a bevitt gének/DNS-darabok előállítása is laboratóriumi úton történik. Egyszerű formái egy gén megismerése után tervezhető meg, majd állítható elő az a változat, ami eddig nem létezett. Elvileg úgy is tekinthetünk erre, mint valamiféle szintetikus allélgyártásra. A cry-gének között ma több olyan található, amelyet ilyen módon állítottak elő, majd a haszonnövény genomjába vitték be. Mai példája ennek a B. thuringiensis var. kumamotoensis szerotípusra visszavezethető cry1A.105 (MON-89034-3 kukorica, MON-87751-7 szója), vagy a B. thuringiensis var. tenebrionis szerotípusra visszavezethető m cry3A-gén (SYN-IR604-5 kukorica).
Valójában a géntechnológiának ez az ága sokkal messzebb tekint: új (a Földön nem létező) örökítőanyag és alternatív örökítés irányában végez kutatásokat (vö. szintetikus biológia). Egyik találata a természetben elő nem forduló bázispárok felfedezése (d5SICS–dNaM). A másik érdeklődése szerint az elvileg létező 172 aminosav közül csak 20-at találunk meg az ismert fehérjékben, vagyis új és eddig ismeretlen fehérjetípusok felfedezése is elképzelhető az ezen a területen kutatók számára. Olyan új bakteriális sejtet (fajt), aminek örökítőanyagát szintetikusan állítottak elő, már létrehoztak.
A következő rész címe: Genomszerkesztés 5 – Géncsendesített élőlények (Biotechnológikaland No44)
Darvas Béla
Bankszámlaszám: 12011265-01425189-00100001
Bank neve: Raiffeisen Bank
Számlatulajdonos: Átlátszónet Alapítvány
1084 Budapest, Déri Miksa utca 10.
IBAN (EUR): HU36120112650142518900400002
IBAN (USD): HU36120112650142518900500009
SWIFT: UBRTHUHB
Számlatulajdonos: Átlátszónet Alapítvány
1084 Budapest, Déri Miksa utca 10.
Bank neve és címe: Raiffeisen Bank
(H-1133 Budapest, Váci út 116-118.)
Támogasd a munkánkat az Átlátszónet Alapítványnak küldött PayPal-adománnyal! Köszönjük.
Támogatom PayPal-adománnyalHa az 1 százalékodat az Átlátszó céljaira, projektjeire kívánod felajánlani, a személyi jövedelemadó bevallásodban az Átlátszónet Alapítvány adószámát tüntesd fel: 18516641-1-42
1% TÁMOGATÁS

(Géntechnologikaland No78) Ukrajnában a GMO-k társadalmi megítélése összességében óvatos, sokszor elutasító. A közvélemény-kutatások és piaci tapasztalatok szerint a lakosság jelentős...

(Biotechnologikaland No77) A Marton Genetics Kft. állásfoglalása A Marton Genetics (Bázismag Kft.) cégcsoport a martonvásári kutatóintézet (Agrártudományi Kutatóközpont) munkájára épült....
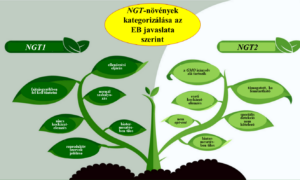
(Biotechnologikaland No76) Előszó A GMO-lobbi hatására az Európai Bizottság javaslata (címábra) komoly visszhangra talált Európában. A javaslatok közül NGT1 esetében...

(Biotechnologikaland No75) Barabás Zoltán Biotechnológiai Egyesület kontra GMO-Kerekasztal A Barabás Zoltán Biotechnológiai Egyesület lépett hazánkban először abból a célból, hogy...
Támogasd a munkánkat banki átutalással. Az adományokat az Átlátszónet Alapítvány számlájára utalhatod. Az utalás közleményébe írd: „Adomány”, köszönjük!